���ڽM�������c�����t�W��3D�����ӡˮ���z���Mչ�c����
3D�����ӡ���gͨ�^���_���Ƽ����ͼ�������|�ɷֵĿ��g�ֲ����阋�����s�����ԽM�������ṩ�˸����Է�����Ȼ�������y��Ȼˮ���z���ڙCе����������ӡ����ȵ͵�ȱ�ݣ����������R�����á��Ϻ���ͨ��W���ٵ��������tԺ���������c�������t��ϵ�y�C����ˮ���z����īˮ�ă������ԣ����ͨ�^���W����{�ͺϵ��ֶ��_�l������ˮ���z����չ������Ƥ�w��ܛ�ǡ����K�ȽM�������еĝ������D1�����о��e���{���ϳ��c����ˮ���z�������ϩ�������zGelMA���Y�Ϲ�̻����g���@��������ӡ�����c�������ԣ�����s�����ؽ��ṩ����˼·��
���P�о��Mչ��“Hydrogels for 3D bioprinting in tissue engineering and regenerative medicine: Current progress and challenges”���}�l����International Journal of Bioprinting��JCR Q1��IF��6.8����

1. ˮ���z����īˮ�ķ���c����
ͨ����ˮ���z�֞���Ȼ�ۺ���纣�����c�����z�����ϳɾۺ������Ҷ���PEG����������Ȼˮ���z����GelMA������ϩ�ữ�����ǣ������ͨ�^�{�������ʯīϩ�ȟo�C/̼�����Ϗͺϣ����@������ˮ���z�ęCе�����c���������ԡ����磬�������c-���z�ͺ�ˮ���z��SA-Gel���Y��nano-ATP���sģ���@���������D2����������Ч���@����ߡ�
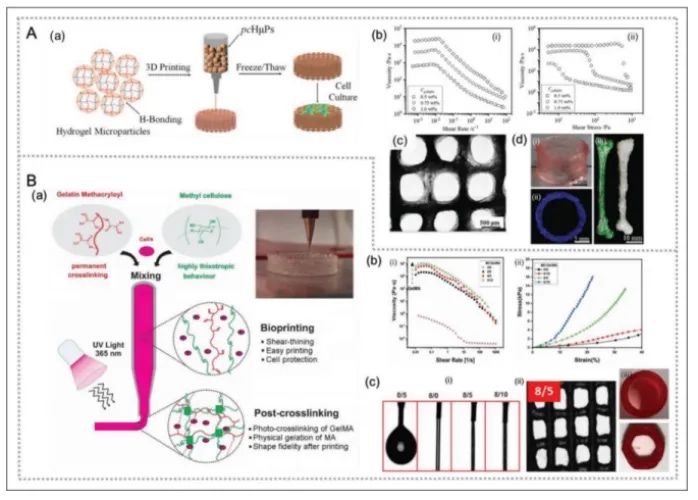
2.�{�ͺ�ˮ���z�Ą�����
�����о��������{�������Laponite���c�������c-PEG�ͺ�ˮ���z�ɴ�ӡ���������ǽY�����䏗��ģ���c��Ȼܛ��ƥ�䣻ʯīϩ�����GO�����sˮ���zͨ�^�{��RANK��̖ͨ·���Mܛ�DZ��o���D3�������⣬��{�װ���GNRs���cGelMA�ͺ�ˮ���z�ɘ������̖�����W�j�������ļ������տs�f�{�ԡ�
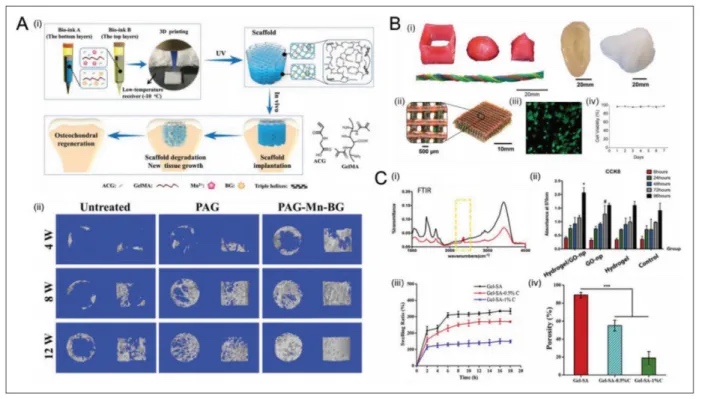
�D3. (A) (i) ʹ��PACG-GelMAˮ���z-Mn²⁺����플Ӻ�PACG-GelMAˮ���z-BG����ӵ�֧�������ӡ��(ii) �ޏ�ܛ��ȱ�p��ʾ��D��(B) PEG-SA-�{�����ˮ���z��3D�����ӡ��(i) ��ͬ�Π��3D�����ӡ�����������w������������Ť���Ķ����Π�ͱ��ӣ�(ii) ʹ�È��g���������ݵ�ˮ���z�W��(iii) HEK�����Ļ����������Ⱦɫ��(iv) 7���HEK�����Ļ��Ԝyԇ��(C) (i) �t����V��ˮ���z���ھ���������GO-np��ˮ���z���t������(ii) ˮ���z��GO-np��ˮ���z/GO-np�Ļ��Ԝyԇ���Լ��հM�е�ܛ�Ǽ�����(iii) ��ӡ����Û�ʣ�(iv) ��̼�{�ܣ�CNTs����Gel-SAˮ���z֧�ܵĿ�϶�ʡ�
3. �R��ǰ���ٴ�ӡͻ��
�F��Y��Ƥ�w����ܡ�����ȹܠ����ټ����K�ȏ��s���ٵ�3D��ӡ�Mչ�����磬ԭλ�����ӡ���g��ֱ���ڄ������ӳ��e���w����-ˮ���z�ͺ������ȫ��Ƥ�wȱ�p���ϣ�����ϩ�����z�ص��ף�Sil-MA��֧�ܳɹ��ޏ��Ú��ȱ�p������ܛ���c��Ƥ�M�������������D4����
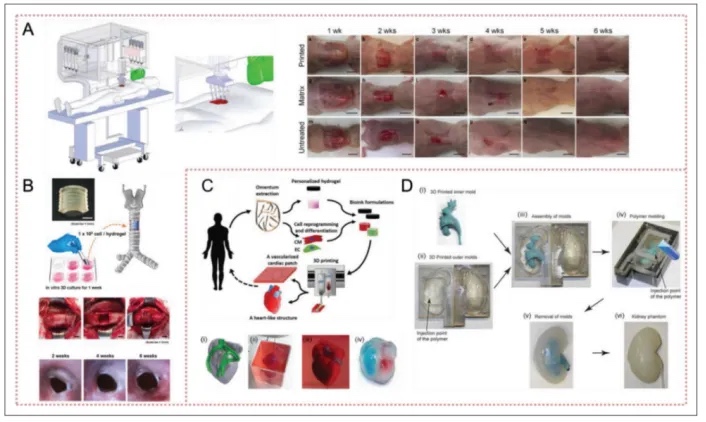
�о����x�cչ��
3D�����ӡ���g�ijɹ����H��ه�ڴ�ӡ��ˇ�c���gƽ�_��߀�߶���ه��������ϵ����܃����ͼ���������á��C��ָ����ˮ���z����һ�N�O�ߝ���������īˮ����ܛӲ�M��������չ�F�ˏV���đ���ǰ����ͨ�^�{�ײ��Ϗͺϡ����滯�W����Լ����������{�أ��о���Ч������ˮ���z�ęCе���ܡ����������Ժͷ����ԡ�Ȼ������ǰ����īˮ�ڝM���ӡ�����c�ṩ�������S�h�����������R����δ�����_�l����ˮ���z����īˮ��������ӡ����������M�������c�R���D���ṩ���ӈԌ���֧�֡��@һ�I��IJ���ͻ�ƣ��،������t�����g�~���¸߶ȣ��邀�Ի��t���������ؽ��_�ُV�ǰ����
ԓ�����@������Ȼ�ƌW����82170694��81700590�����Ϻ���ͨ��W“�t���������”��YG2022ZD020�����Y����
����朽�: https://doi.org/10.18063/ijb.759
(؟�ξ���admin)
��һƪ����cNCDMM����Aheadd CP1���Ƅ��X�Ͻ�3D��ӡ�ڇ��������I�����
- ����cNCDMM����Aheadd CP1���Ƅ��X��
- �����ڽM�������c�����t�W��3D�����ӡˮ
- ����e��ԇ�e����������AI�㷨5���i��3D
- �������3D��ӡ-īˮֱ����Nature Review
- ���Ͽƴ�-�����Ժʿ ��:�������Ϻ���
- ��Ad-Proc-Add II������3D��ӡ늻��W��̎
- ��dditive Appearance�Ƴ������3D��ӡܛ
- ����ِ��������������|��Ώ�3D��ӡِ
- ��3D��ӡ�մɼ��g���IJ��ϸ��µ����I��
- �����A�Cеϵ�����������ĈF����¸��о�
- ���������ӌW����ܵ���������TC4��ˇ��
- ���p���Ӿۺϡ��߾��������I��ġ����ǡ�
- ��3D��ӡ����Y���OӋ�K�Oָ�ϣ������p��
- ���C���������·���3D��ӡ���g
- ���B�m�����̼��g����ͻ�ƣ�Carbon����
- ��3D�����ӡ���g����������ٹ����е���
- ���u݆�~Ƭ�����������������ޏͼ��g����
- ���Gɫ�ְ�ȫ��3D��ӡ�zԭˮ���z���IJ���
- ��3D��ӡ�C���g���ƴ��FDM��SLA��CLIP��
- ���P�c2024��ʮƪ�l����Science��Nature


 ��cNCDMM����Aheadd CP
��cNCDMM����Aheadd CP ��e��ԇ�e����������AI��
��e��ԇ�e����������AI�� �����3D��ӡ-īˮֱ����N
�����3D��ӡ-īˮֱ����N �Ͽƴ�-�����Ժʿ ��:
�Ͽƴ�-�����Ժʿ ��: Ad-Proc-Add II������3D��
Ad-Proc-Add II������3D�� ͻ��������3D��ӡ
ͻ��������3D��ӡ �ϰ�LEAP 71��˾
�ϰ�LEAP 71��˾ 3D�����ӡ������
3D�����ӡ������ ��Small Science
��Small Science ��������-�����
��������-����� ���A��W��������
���A��W��������

